SILVER SPRING, Maryland, EUA: A Food and Drug Administration (FDA) dos EUA finalizou as diretrizes sobre estudos em animais para dispositivos de materiais para enxerto ósseo dentário, com o objetivo de reduzir a dependência de testes em animais em submissões pré-comercialização. Publicado em agosto de 2025, o documento atualiza as diretrizes anteriores de 2005 e visa refletir as práticas de revisão atuais, promover a consistência e agilizar a avaliação das submissões.
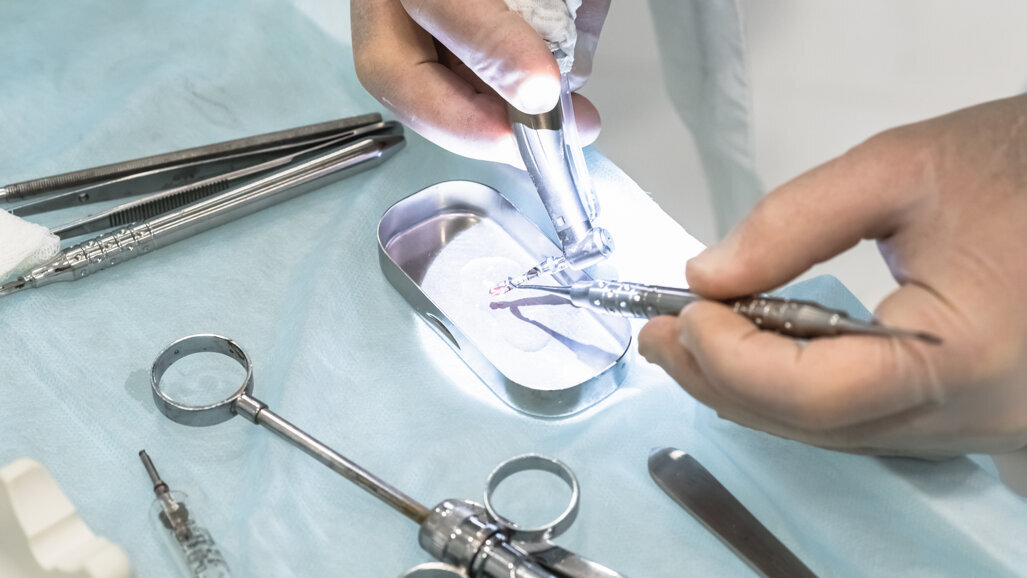
A agência publicou pela primeira vez uma versão preliminar do documento em março de 2024. O documento de orientação final estabelece recomendações detalhadas para estudos em animais que podem ser usadas para demonstrar a conformidade com controles especiais aplicáveis a dispositivos de enxerto ósseo dentário. Ele descreve considerações como a seleção de locais anatômicos consistentes com o uso intraoral pretendido ou o uso de modelos de defeitos de pior caso.
Em entrevista ao Dental Tribune International, a FDA enfatizou que o documento serve como um recurso para fabricantes que desenvolvem biomateriais novos ou inovadores, auxiliando-os a avaliar a segurança e o desempenho para submissões de marketing. Para empresas que ainda realizam testes em animais, as recomendações visam garantir o fornecimento de dados in vivo adequados . Ao mesmo tempo, a FDA incentiva os patrocinadores a consultar a agência caso desejem utilizar alternativas validadas e sem uso de animais.
“A FDA acredita que as recomendações detalhadas de estudos em animais fornecidas nesta orientação podem ajudar os fabricantes a fornecer dados adequados de estudos em animais, quando um estudo em animais é conduzido para dar suporte a uma submissão 510(k) para dispositivos de material de enxerto ósseo dentário”, disse um porta-voz da FDA ao Dental Tribune International.
Um foco central do documento é o apoio aos 3Rs: substituir, reduzir e refinar o uso de animais. A FDA observou que o documento pode ajudar a reduzir o número de animais necessários, combinando estudos de segurança e desempenho com testes de biocompatibilidade em um único projeto.
Garantir padrões de segurança, desempenho e testes éticos
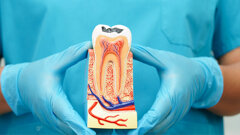
O enxerto ósseo tem se tornado cada vez mais comum na odontologia devido aos avanços na medicina regenerativa, ao desenvolvimento de novos biomateriais e à crescente demanda por restauração óssea. De acordo com um estudo de 2021, até metade de todos os procedimentos de implante envolvem enxerto, totalizando aproximadamente 2,2 milhões de procedimentos realizados em todo o mundo a cada ano. 1 Embora os autoenxertos continuem sendo o padrão ouro, os xenoenxertos provenientes de osso bovino e suíno são amplamente utilizados. 2
Ao finalizar este documento de orientação, o FDA busca fornecer aos fabricantes maior clareza, apoiar a inovação em biomateriais odontológicos e incentivar a adoção de abordagens de teste que garantam segurança e desempenho, ao mesmo tempo que limitam o uso em animais.
TAIYUAN, China: Nas últimas semanas, começaram a surgir detalhes de uma investigação sobre um comércio perturbador e altamente lucrativo de partes de ...
ZURIQUE, Suíça: A startup suíça Odne anunciou recentemente que recebeu autorização de mercado da Food and Drug Administration (FDA) dos EUA para seu ...
SILVER SPRING, Maryland, EUA: No dia 21 de Janeiro, a FDA- Food and Drug Administration (Administração de Alimentos e Medicamentos dos EUA) ...
VANCOUVER, British Columbia, Canada: Devido às potenciais complicações associadas aos autoenxertos, existe a necessidade de estruturas de tecido ósseo ...
HONG KONG, China/BERKELEY, Califórnia, EUA: Um estudo conduzido por pesquisadores na China examinou recentemente o impacto da microbiota oral na saúde ...
GIESSEN, Alemanha: Para expandir o acesso ao atendimento pediátrico para além do ambiente clínico tradicional, a aplicação da teleodontologia ...
GOLD COAST, Austrália: O alto nível socioeconômico tem sido frequentemente associado a melhores resultados de saúde. No entanto, de acordo com um estudo...
SILVER SPRING, Md., EUA: A FoodandDrugAdministration (FDA sigla em inglês) dos EUA anunciou recentemente que medicamentos contendo buprenorfina que são ...
COPENHAGEN, Dinamarca: O desgaste dentário erosivo (ETW) é uma preocupação crescente para os profissionais da área odontológica e, portanto, objeto de...
ANKARA, Turquia: O uso de implantes dentários padrão tornou-se uma modalidade de tratamento amplamente aceita para a reabilitação do edentulismo ...
Webinar ao vivo
seg. 13 abril 2026
14:00 BRT (Sao Paulo)
Dr. David Norré, Dr. Tommie Van de Velde DDS, MSc, PhD
Webinar ao vivo
ter. 14 abril 2026
21:00 BRT (Sao Paulo)
Dr. Bruce McFarlane Certified Specialist in Orthodontics Fellow: Royal College of Dentists of Canada Diplomate: American Board of Orthodontics
Webinar ao vivo
qua. 15 abril 2026
15:00 BRT (Sao Paulo)
Webinar ao vivo
qua. 15 abril 2026
21:00 BRT (Sao Paulo)
Linda Hecker MS, BSDH, RDH
Webinar ao vivo
qui. 16 abril 2026
13:00 BRT (Sao Paulo)
Dr. Pär-Olov Östman, Dr. Robert Gottlander DDS
Webinar ao vivo
sex. 17 abril 2026
13:00 BRT (Sao Paulo)
Webinar ao vivo
sex. 17 abril 2026
14:00 BRT (Sao Paulo)
Dr. Stuart Yeaton BDentSc, MOrth



 Áustria / Österreich
Áustria / Österreich
 Bósnia e Herzegovina / Босна и Херцеговина
Bósnia e Herzegovina / Босна и Херцеговина
 Bulgária / България
Bulgária / България
 Croácia / Hrvatska
Croácia / Hrvatska
 República Checa; Eslováquia / Česká republika & Slovensko
República Checa; Eslováquia / Česká republika & Slovensko
 França / France
França / France
 Alemanha / Deutschland
Alemanha / Deutschland
 Grécia / ΕΛΛΑΔΑ
Grécia / ΕΛΛΑΔΑ
 Hungria / Hungary
Hungria / Hungary
 Itália / Italia
Itália / Italia
 Países Baixos / Nederland
Países Baixos / Nederland
 Países Nórdicos / Nordic
Países Nórdicos / Nordic
 Polónia / Polska
Polónia / Polska
 Portugal / Portugal
Portugal / Portugal
 Roménia; Moldávia / România & Moldova
Roménia; Moldávia / România & Moldova
 Eslovénia / Slovenija
Eslovénia / Slovenija
 Sérvia; Montenegro / Србија и Црна Гора
Sérvia; Montenegro / Србија и Црна Гора
 Espanha / España
Espanha / España
 Suíça / Schweiz
Suíça / Schweiz
 Turquia / Türkiye
Turquia / Türkiye
 Reino Unido e Irlanda / UK & Ireland
Reino Unido e Irlanda / UK & Ireland
 Internacional / International
Internacional / International
 Canadá / Canada
Canadá / Canada
 América Latina / Latinoamérica
América Latina / Latinoamérica
 EUA / USA
EUA / USA
 China / 中国
China / 中国
 Índia / भारत गणराज्य
Índia / भारत गणराज्य
 Paquistão / Pākistān
Paquistão / Pākistān
 Vietname / Việt Nam
Vietname / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Argélia, Marrocos e Tunísia / الجزائر والمغرب وتونس
Argélia, Marrocos e Tunísia / الجزائر والمغرب وتونس
 Médio Oriente / Middle East
Médio Oriente / Middle East







































To post a reply please login or register