SILVER SPRING, Maryland, EUA: A Administração de Alimentos e Medicamentos dos EUA (FDA) anunciou novas medidas de fiscalização para restringir a venda de medicamentos com flúor ingerível para crianças. Essa medida visa orientar os fabricantes a interromper a comercialização de produtos rotulados para uso em crianças menores de 3 anos e em crianças maiores que não apresentem alto risco de cárie dentária. A decisão é resultado de uma avaliação científica formal dos suplementos de flúor utilizados na população pediátrica e de meses de consulta pública. Ela representa uma mudança significativa na supervisão federal de produtos que foram prescritos por décadas sem terem passado por uma avaliação completa da FDA quanto à segurança, eficácia ou qualidade de fabricação.
Produtos de flúor de prescrição médica, com um único ingrediente, para ingestão — geralmente fornecidos como gotas orais ou comprimidos mastigáveis com doses diárias entre 0,25 mg e 1,0 mg — são usados nos EUA desde a década de 1940, principalmente para crianças que vivem em áreas sem água com níveis ideais de fluoretação. No entanto, com base em sua revisão mais recente, a única desse tipo desde a década de 1940, o FDA concluiu que esses suplementos não devem ser usados em crianças menores de 3 anos e devem ser limitados a crianças mais velhas com alto risco de cárie. Notificações foram enviadas às empresas que não seguem essas diretrizes.
Benefício limitado para dentes decíduos, preocupação com riscos à saúde.
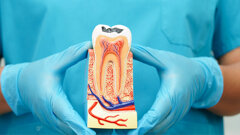
A avaliação científica da FDA e as revisões independentes citadas relatam que os ensaios clínicos existentes fornecem pouca ou nenhuma evidência de que os suplementos de flúor ingeríveis reduzam a cárie em dentes decíduos, embora indiquem algum benefício em dentes permanentes. Além disso, as descobertas mostram que o uso de suplementos de flúor em crianças muito pequenas aumenta o risco de fluorose dentária e que a suscetibilidade atinge o pico no segundo ano de vida.
A FDA também observou preocupações decorrentes de estudos recentes que sugerem potenciais efeitos da maior exposição ao flúor no desenvolvimento neurológico e possível alteração da microbiota intestinal, e enfatizou que, embora esses dados sejam preliminares, exigem cautela. Com base nisso, a agência acredita que os potenciais danos de produtos com flúor ingeríveis não aprovados para crianças pequenas podem superar seus benefícios comprovados.
Respostas profissionais e de defesa
A decisão da FDA coincide com orientações de longa data de órgãos profissionais que apoiam a suplementação sistêmica de flúor para crianças em áreas onde a água não é fluoretada. A Associação Americana de Odontologia, em uma resposta inicial, reafirmou o apoio ao uso de flúor baseado em evidências e enfatizou que os profissionais de saúde devem manter a flexibilidade para prescrever suplementos para pacientes de alto risco adequadamente selecionados.
“O julgamento clínico do médico, e não um novo aviso na embalagem, deve continuar sendo o fator determinante para definir o uso adequado de flúor em crianças, garantindo tanto a segurança quanto o acesso a cuidados essenciais de saúde bucal”, afirmou o Dr. Richard J. Rosato, presidente da Associação Americana de Odontologia, em um comunicado à imprensa. Ao mesmo tempo, alguns defensores da saúde bucal alertaram que controles mais rígidos sobre suplementos, combinados com a redução da fluoretação da água potável em algumas regiões dos EUA, podem agravar problemas já existentes na saúde bucal pediátrica, caso não sejam acompanhados por um acesso ampliado a cuidados preventivos alternativos.
Contexto global e político
Internacionalmente, as políticas de fluoretação da água potável permanecem heterogêneas. Vários países europeus recorrem a estratégias alternativas, como a fluoretação do sal ou programas odontológicos públicos abrangentes, enquanto a Organização Mundial da Saúde recomenda atualmente uma concentração de flúor de até 1,5 mg/l na água potável, sendo que cerca de 0,7 mg/l é frequentemente citado como eficaz para a prevenção da cárie.
Desenvolvimentos legislativos recentes nos EUA, incluindo proibições estaduais da fluoretação da água potável em Utah e na Flórida, intensificaram ainda mais o debate sobre a exposição sistêmica ao flúor e a necessidade de estratégias preventivas robustas e equitativas para crianças.
Próximos passos para a pesquisa e a prática
A FDA, juntamente com os Institutos Nacionais de Saúde (NIH) e o Departamento de Saúde e Serviços Humanos (HHS), planeja implementar uma agenda de pesquisa direcionada e uma estratégia nacional mais ampla de saúde bucal para abordar as lacunas de evidências relacionadas à exposição ao flúor e seus efeitos em crianças. Essa ação sinaliza uma recalibração do uso sistêmico de flúor na primeira infância e ressalta a importância de alinhar as práticas preventivas de longa data com as evidências e normas regulatórias atuais. Os profissionais da odontologia desempenharão um papel central na interpretação das recomendações à medida que evoluem e na garantia do acesso à prevenção eficaz e baseada em evidências científicas da cárie para as crianças mais necessitadas.
CHICAGO, EUA: Dependência de opióides pode bem ser uma das mais prementes questões relacionadas com a toxicodependência da comunidade global atualmente....
BOSTON, EUA: Entre os inúmeros aspectos controversos do atual mandato de Donald Trump como presidente dos EUA, o compromisso do Secretário de Saúde e ...
LEIPZIG, Alemanha: Comunidades rurais nos EUA enfrentam uma crescente crise de saúde bucal, com a diminuição do acesso à água fluoretada e aos cuidados...
CHICAGO, EUA: O Instituto de Política de Saúde da Associação Odontológica Americana (ADA) descobriu que o declínio da matrícula em programas de ...
EFFINGHAM, Illinois, EUA: A crescente força das organizações de apoio odontológico (DSOs, na sigla em inglês) na América do Norte está transformando ...
ROCK HILL, Carolina do Sul, EUA: A 3D Systems anunciou o lançamento comercial nos EUA de sua solução de próteses totais NextDent Jetted Denture ...
SILVER SPRING, Md., EUA: A Administração de Medicamentos e Alimentos (FDA- sigla em inglês) propôs recentemente a redução do nível permitido de ...
CHICAGO, EUA: O Instituto de Ciência e Pesquisa da Associação Dentária Americana (ADA) e a Faculdade de Medicina Dentária da Universidade de ...
GENEBRA, Suíça: A FDI World Dental Federation tem o prazer de informar que um rascunho atualizado do Plano de Ação Global de Saúde Oral (2023–2030) ...
WASHINGTON, EUA: A American Dental Association (ADA) e 19 outras associações de assistência médica instaram os legisladores dos EUA a enfrentar os ...
Webinar ao vivo
qui. 2 abril 2026
13:00 BRT (Sao Paulo)
Webinar ao vivo
qua. 8 abril 2026
14:00 BRT (Sao Paulo)
Webinar ao vivo
qui. 9 abril 2026
14:00 BRT (Sao Paulo)
Webinar ao vivo
qui. 9 abril 2026
15:00 BRT (Sao Paulo)
Prof. Moritz Kebschull, Cat Edney
Webinar ao vivo
sex. 10 abril 2026
11:00 BRT (Sao Paulo)
Webinar ao vivo
sex. 10 abril 2026
12:00 BRT (Sao Paulo)
Dr. med. dent. Henrik-Christian Carl Hollay
Webinar ao vivo
sex. 10 abril 2026
13:00 BRT (Sao Paulo)
Prof. Dr. Ali Murat Kökat



 Áustria / Österreich
Áustria / Österreich
 Bósnia e Herzegovina / Босна и Херцеговина
Bósnia e Herzegovina / Босна и Херцеговина
 Bulgária / България
Bulgária / България
 Croácia / Hrvatska
Croácia / Hrvatska
 República Checa; Eslováquia / Česká republika & Slovensko
República Checa; Eslováquia / Česká republika & Slovensko
 França / France
França / France
 Alemanha / Deutschland
Alemanha / Deutschland
 Grécia / ΕΛΛΑΔΑ
Grécia / ΕΛΛΑΔΑ
 Hungria / Hungary
Hungria / Hungary
 Itália / Italia
Itália / Italia
 Países Baixos / Nederland
Países Baixos / Nederland
 Países Nórdicos / Nordic
Países Nórdicos / Nordic
 Polónia / Polska
Polónia / Polska
 Portugal / Portugal
Portugal / Portugal
 Roménia; Moldávia / România & Moldova
Roménia; Moldávia / România & Moldova
 Eslovénia / Slovenija
Eslovénia / Slovenija
 Sérvia; Montenegro / Србија и Црна Гора
Sérvia; Montenegro / Србија и Црна Гора
 Espanha / España
Espanha / España
 Suíça / Schweiz
Suíça / Schweiz
 Turquia / Türkiye
Turquia / Türkiye
 Reino Unido e Irlanda / UK & Ireland
Reino Unido e Irlanda / UK & Ireland
 Internacional / International
Internacional / International
 Canadá / Canada
Canadá / Canada
 América Latina / Latinoamérica
América Latina / Latinoamérica
 EUA / USA
EUA / USA
 China / 中国
China / 中国
 Índia / भारत गणराज्य
Índia / भारत गणराज्य
 Paquistão / Pākistān
Paquistão / Pākistān
 Vietname / Việt Nam
Vietname / Việt Nam
 ASEAN / ASEAN
ASEAN / ASEAN
 Israel / מְדִינַת יִשְׂרָאֵל
Israel / מְדִינַת יִשְׂרָאֵל
 Argélia, Marrocos e Tunísia / الجزائر والمغرب وتونس
Argélia, Marrocos e Tunísia / الجزائر والمغرب وتونس
 Médio Oriente / Middle East
Médio Oriente / Middle East



































To post a reply please login or register